Quá Trình Đẳng Nhiệt – Định Luật Bôi-Lơ Ma-Ri-Ốt
Một trong những nội dung trọng tâm mà các em sẽ được học trong chương trình Vật Lý lớp 10 đó chính là quá trình đẳng nhiệt – định luật Bôi-Lơ Ma-Ri-Ốt. Để giúp các em nắm vững kiến thức này tốt hơn, Marathon Education đã tổng hợp một số lý thuyết quan trọng liên quan đến quá trình đẳng nhiệt mà các em cần nắm vững và chia sẻ qua bài viết dưới đây. Các em hãy cùng theo dõi và học tập nhé!
Trạng thái và quá trình biến đổi trạng thái của chất khí
Theo cách thông thường, trạng thái của một chất khí bất kỳ được xác định qua 3 thông số sau đây:
- Áp suất (p), đơn vị đo là N/m2, Pa, atm, mmHg…
- Thể tích (V), đơn vị đo là l hoặc m3
- Nhiệt độ tuyệt đối (T), đơn vị đo là độ C và tính theo công thức T = 273 + t (với t là nhiệt độ Xen-xi-út)
Đây là các thông số chính của trạng thái chất khí, giữa các thông số này thường có những mối liên hệ xác định.
Trong quá trình tự nhiên, 3 thông số đều sẽ thay đổi liên tục. Nếu một trong 3 thông số thay đổi thì trạng thái khí cũng sẽ thay đổi tức thì. Quá trình thay đổi này được gọi là quá trình biến đổi trạng thái khí. Đặc biệt, trong trường hợp 2 thông số biến đổi và 1 thông số giữ nguyên thì quá trình này gọi là quá trình đẳng nhiệt.
Định luật Bôi-lơ Ma-ri-ốt
Quá trình đẳng nhiệt là gì?
Quá trình biến đổi trạng thái nhưng nhiệt độ vẫn được giữ nguyên, ta gọi đó là quá trình đẳng nhiệt.
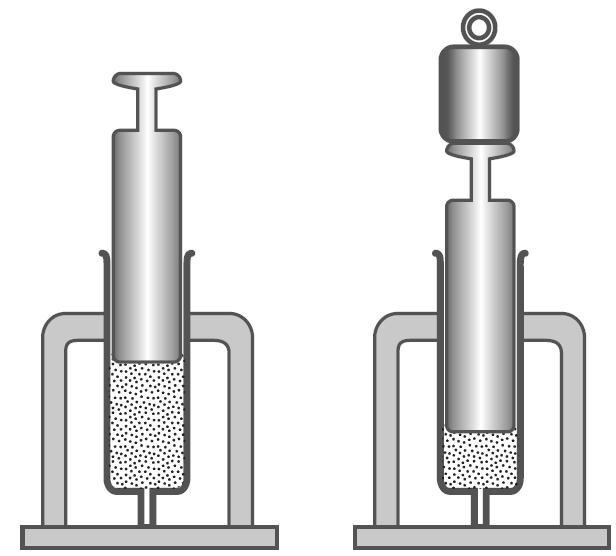
Ví dụ: Một ống xilanh chứa không khí ở áp suất và nhiệt độ thấp. Các em dùng tay nén chậm chậm piston để làm giảm thể tích khí và áp suất khí thay đổi. Quá trình này ta gọi là quá trình đẳng nhiệt.
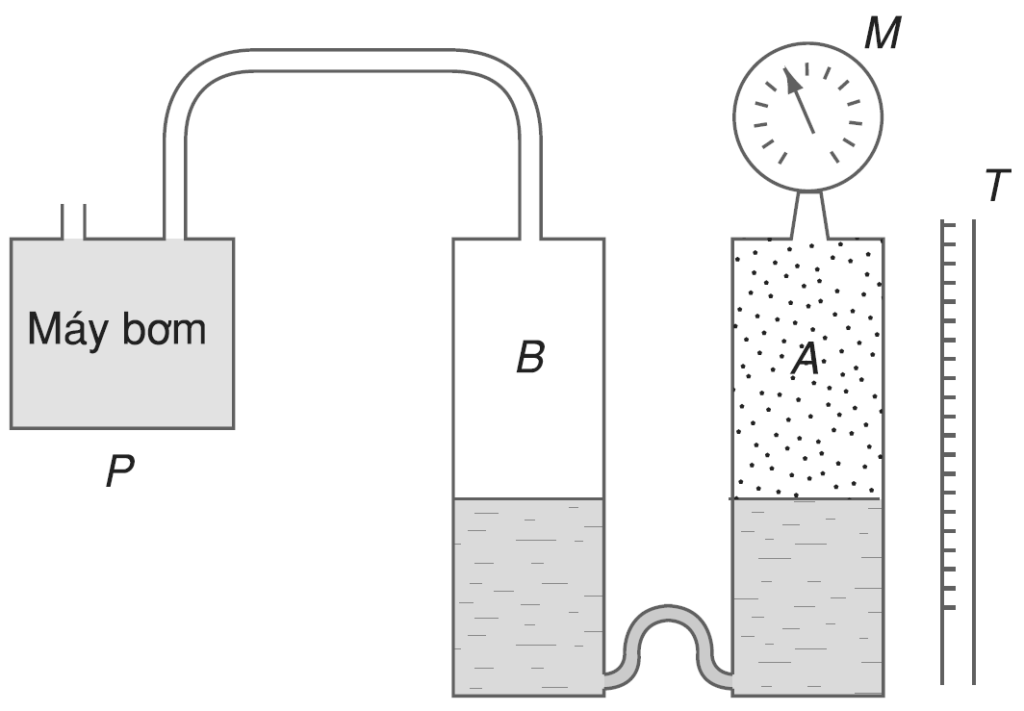
Các em tiến hành thí nghiệm thay đổi thể tích của một lượng khí, đo áp suất tương ứng với mỗi thể tích ta có kết quả như sau:
| Thể tích V (cm3) | Áp suất P (105 Pa) | pV |
| 20 | 1.00 | 2 |
| 10 | 2.00 | 2 |
| 40 | 0.5 | 2 |
| 30 | 0.67 | 2 |
⟹ Qua thí nghiệm trên ta thấy được, trong quá trình đẳng nhiệt của của một lượng khí thì áp suất tỉ lệ nghịch với thể tích.
Định luật Bôi-lơ Ma-ri-ốt
Phát biểu định luật: Trong quá trình đẳng nhiệt của 1 lượng khí nhất định thì áp suất (p) tỉ lệ nghịch với thể tích (V).
Định luật Bôi-lơ Ma-ri-ốt được Nhà vật lý thiên tài người Anh Bôi-lơ (1627 – 1691) khởi xướng năm 1662 và nhà vật lý người Pháp Ma-ri-ốt (1620 – 1684) cũng tìm ra định lý tương tự năm 1676 nên định luật này mới có tên gọi là Bôi-lơ Ma-ri-ốt.
Công thức đẳng nhiệt
pV = const (hằng số) hay p ~ 1V
Trong đó:
- p là áp suất (pa)
- V là thể tích (cm3)
Nếu các em gọi p1, V1 là áp suất và thể tích của một lượng khí ở trạng thái 1 và p2, V2 là áp suất và thể tích của lượng khí ở trạng thái 2, thì theo định luật Bôi-lơ Ma-ri-ốt ta được:
p1V1 = p2V2
Đường đẳng nhiệt
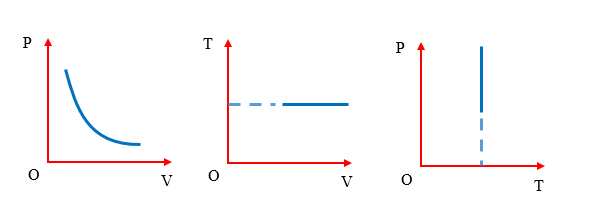
Đường biểu diễn sự biến thiên của áp suất một lượng khí theo thể tích được gọi là đường đẳng nhiệt.
Trong hệ tọa độ (pOV) thì đường đẳng nhiệt được biểu diễn là một đường cong hypebol. Đường đẳng nhiệt ở trên ứng với nhiệt độ cao sẽ nằm ở vị trí hơn đường đẳng nhiệt ở dưới.
Tham khảo ngay các khoá học online của Marathon Education
Với những nội dung chia sẻ ở trên, Marathon Education mong rằng đã giúp các em nắm vững những kiến thức liên quan đến quá trình đẳng nhiệt – định luật Bôi-Lơ Ma-Ri-Ốt chương trình Lý 10. Qua đó, các em dễ dàng giải thích một số hiện tượng có trong tự nhiên và giải các bài tập liên quan. Ngoài ra, các em hãy theo dõi website của Marathon để có thể học trực tuyến nhiều kiến thức cơ bản Toán – Lý – Hóa – Văn khác. Chúc các em học tập tốt và luôn đạt thành tích cao trong kì thi sắp tới!