Lý Thuyết Ankadien Hóa 11: Định Nghĩa, Tính Chất Và Điều Chế Ankadien
Ankadien với phản ứng trùng hợp đã tạo ra nhiều hợp chất có tính đàn hồi cao như cao su và có nhiều ứng dụng ở nhiều lĩnh vực trong đời sống. Vậy Ankadien là gì? Hợp chất này có tính chất hóa học và phương pháp điều chế như thế nào? Các em hãy cùng Marathon Education tìm hiểu chi tiết hơn về những lý thuyết này qua bài viết dưới đây.
>>> Xem thêm: Lý Thuyết Ankan: Định Nghĩa, Danh Pháp, Công Thức Của Ankan
Định nghĩa Ankadien
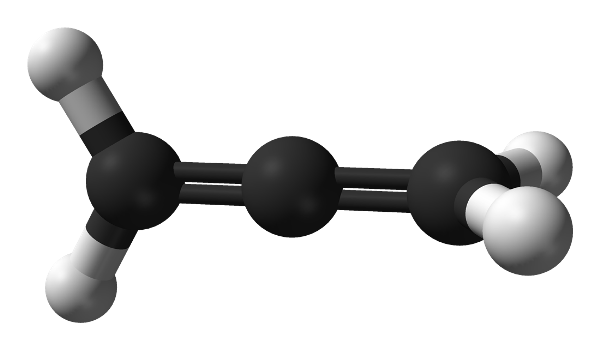
Ankadien được định nghĩa là hidrocacbon mạch hở, không no. Trong phân tử hợp chất này có chứa 2 liên kết đôi và có công thức tổng quát là CnH2n-2 (với n≥ 3).
Ví dụ:
CH2 = C = CH2: propadien
CH2 – C = CH – CH3: buta -1,2 – dien
CH2 = CH – CH = CH2: buta -1,3 – dien
Công thức tổng quát của Ankadien liên hợp: CnH2n-2 (với n≥ 4).
Cách gọi tên Ankadien tổng quát như sau: số chỉ vị trí nhánh – tên nhánh + tên mạch chính + a – số chỉ vị trí nối đôi – dien
>>>Xem thêm: Lý Thuyết Anken: Khái Niệm, Danh Pháp Và Phản Ứng Đặc Trưng Của Anken
Phân loại Ankadien
Dựa vào vị trí liên kết đôi, các em có thể chia Ankadien thành 3 loại:
- Ankadien có 2 liên kết đôi ngay cạnh nhau: CH2 = C = CH2.
- Ankadien liên hợp (có liên kết đôi cách nhau bởi 1 liên kết đơn): CH2 = CH – CH = CH2.
- Ankadien có 2 liên kết đôi cách nhau từ 2 liên kết đơn trở lên: CH2 = CH – CH2 – CH = CH2.
>>> Xem thêm: Lý Thuyết Ankin: Khái Niệm, Tính Chất Lý Hóa Và Cách Điều Chế Ankin
Tính chất hóa học của Ankadien

Phản ứng cộng
Ankadien cộng với Hidro (H2) với chất xúc tác là Niken và nhiệt độ.
CH_2=CH-CH=CH_2 + 2H_2\xrightarrow{t^o,\ Ni} CH_3-CH_2-CH_2-CH_3
Ankadien cộng Brom (Br2)
- Cộng 1,2 ở nhiệt độ 800C:
CH_2 = CH - CH = CH_2 + Br_2 \xrightarrow{80^oC} CH_2Br-CHBr-CH=CH_2
- Cộng 1,4 ở nhiệt độ 400C:
CH_2 = CH - CH = CH_2 + Br_{2\ (dd)} \xrightarrow{40^oC} CH_2Br - CH = CH - CH_2Br
- Cộng vào cả 2 liên kết đôi:
CH_2 = CH - CH = CH_2 + 2Br_{2\ (dd)} \to CH_2Br - CHBr - CHBr - CH_2Br
Hiện tượng: làm mất màu dung dịch Br2.
Ankadien cộng Hidro Halogenua (HBr)
- Cộng 1,2 ở nhiệt độ -800C:
CH_2 = CH - CH = CH_2 + HBr \xrightarrow{80^oC} CH_3 - CH_2 - CHBr - CH_3
- Cộng 1,4 ở nhiệt độ 400C:
CH_2 = CH - CH = CH_2 + HBr \xrightarrow{40^oC} CH_3 - CH = CH - CH_2Br \small\text{ (sản phẩm chính)}
Phản ứng trùng hợp
buta – 1,3 – đien hay C4H8 phản ứng trùng hợp khi có mặt kim loại Natri hoặc chất xúc tác khác (trùng hợp theo kiểu 1,4) để tạo thành polibutađien.
nCH_2=CH-CH=CH_2\xrightarrow{t^o,\ p,\ xt}\sout{\ (\ }CH_2-CH=CH-CH_2\sout{\ )\ }_n
Phản ứng oxi hóa
Phản ứng oxi hóa hoàn toàn, có xúc tác của nhiệt độ
2C_4H_6 + 11O_2 \xrightarrow{t^o} 8CO_2 + 6H_2O
Phản ứng oxi hóa không hoàn toàn
3C_4H_6 + 8H_2O + 4KMnO_4 —> 3C_4H_6(OH)_4 + 4KOH + 4MnO_2
Qua 2 phản ứng trên, để nhận biết Ankadien các em có thể dùng dung dịch Brom hoặc KMnO4.
>>> Xem thêm: Lý Thuyết Về Oxi Và Tính Chất Hóa Học Của Oxi Hóa Lớp 10
Cách điều chế ankadien
Để điều chế được Ankadien, các em có thể tiến hành theo hai cách sau:
Cách 1: Điều chế butilen hoặc buta – 1,3 – dien từ butan bằng cách đề hidro hóa
CH_3-CH_2-CH_2-CH_3\xrightarrow{t^o,\ xt}CH_2=CH-CH=CH_2+2H_2
Cách 2: Điều chế isopren bằng cách tách hidro của isopentan
CH_3-CH(CH_3)-CH_2-CH_3\xrightarrow{t^o,\ xt}CH_2=C(CH_3)-CH=CH_2+2H_2
Ứng dụng của ankadien
- Dùng buta-1,3-dien hoặc isopren để điều chế polibutadien hoặc poliisopren, là những tính chất có đàn hồi cao
- Dùng để sản xuất cao su (lốp xe, nhựa trám thuyền,..)
Một số bài tập Ankadien
Giải bài tập 2 SGK trang 135
\begin{aligned}
&Viết\space phương\space trình\space hóa\space học\space (ở\space dạng\space công\space
thức\space cấu\space tạo)\space của\space các\space phản\space ứng\space xảy\space ra\space khi:\\
&a.\space Isopren\space tác\space dụng\space với\space hidro\space (xúc\space tác\space Ni)\\
&b.\space Isopren\space tác\space dụng\space với\space brom\space trong\space (trong\space CCl_4)\\
&Các\space chất\space được\space lấy\space theo\space tỉ\space lệ\space số\space mol\space 1 : 1 \space tạo\space a\space sản\space phẩm\space theo\space kiểu\space cộng\space 1, 4.\\
&c.\space Trùng \space hợp\space isopren\space theo\space kiểu\space 1,4.
\end{aligned}
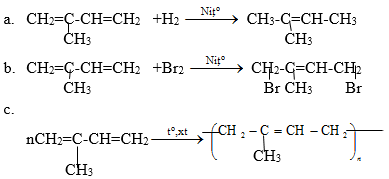
Giải bài tập 3 SGK trang 135
\begin{aligned}
& Oxi\space hóa \space hoàn\space toàn\space 0,680\space gam\space ankadien\space X\space thu\space được\space 1,120\space lít\space CO_2 \space (đktc)\\&a)Tìm\space công\space thức\space phân\space tử\space của\space X\\&b)Tìm\space công\space thức\space cấu\space tạo\space có\space thể\space có\space của\space X
\end{aligned}
\begin{aligned}
&a)Gọi\space công\space thức\space phân\space tử\space của\space ankadien\space X\space là\space C_nH_{2n-2}\space (n\ge3)\\&-Theo\space bài\space ra,\space khi\space oxi\space hóa\space hoàn\space toàn\space 0,68gam\space X\space thu\space được\space 1,120\space lít\space CO_2\space (đktc)\\&n_{CO_2}=\frac{V}{22,4}=\frac{1,12}{22,4}=0,05(mol)\\&-Gọi\space a\space là\space số\space mol\space của\space ankadien\space X, phương\space trình\space oxi\space hoàn\space toàn\\&C_nH_{2n-2}+[\frac{(3n-1)}{2}]\to nCO_2+(n-1)H_2O\\&a.n(mol)\\& -Theo\space bài\space ra,\space oxi\space hóa\space hoàn\space toàn\space 0,68\space X\space nên\space ta\space có:\\&m_x=(14n-2)a=0,68\space (*) \\&-Theo\space PTPƯ\space và\space bài\space ra,số\space mol\space CO_2\space là: n_{CO_2}=a.n=0.05\space (**)\\&-Từ (*)\space và\space (**)\space ta\space giải\space được\space: n=5\space và\space n=0.01.\\&\Rightarrow X\space có\space công\space thức\space phân\space tử\space là:C_5H_8\\&b)Tìm\space công\space thức\space cấu\space tạo\space có\space thể\space có\space của\space C_5H_8 là:\\&CH_2=CH-CH=CH-CH_3\\&CH2=CH-CH_2-CH=CH_2\\&CH_2=C=CH-CH_2-CH_3\\&CH_3-CH=C=CH-CH_3\\&CH_2=C(CH_3)-CH=CH_2
\end{aligned}
Tham khảo ngay các khoá học online của Marathon Education
Trên đây là những chia sẻ của team Marathon Education về lý thuyết về Ankadien Hóa 11, cũng như tính chất và cách điều chế hợp chất này. Các em hãy tham khảo thật kỹ để có thể nắm bắt hết mọi kiến thức nêu trên nhằm phục vụ tốt quá trình học tập của bản thân. Ngoài ra, các em cũng có thể theo dõi website của Marathon để học trực tuyến nhiều kiến thức khác. Chúc các em học tập vui vẻ và đạt nhiều thành tích cao trong mọi cuộc thi!
Các Bài Viết Liên Quan