Lý Thuyết Anken: Khái Niệm, Danh Pháp Và Phản Ứng Đặc Trưng Của Anken
Trong Hóa học, anken là một khái niệm cơ bản, các em cần nắm rõ các tính chất vật lý, hóa học của nó để ứng dụng vào giải bài tập tốt hơn. Hãy cùng Marathon Education tìm hiểu rõ về khái niệm, danh pháp và tính chất của anken trong bài viết sau!
>>> Xem thêm: Lý Thuyết Ankin: Khái Niệm, Tính Chất Lý Hóa Và Cách Điều Chế Ankin
Tổng quát về anken
Anken là gì?

Anken là hiđrocacbon không no, mạch hở trong phân tử có chứa các liên kết đơn và 1 liên kết đôi C=C.
Hợp chất có công thức đơn giản nhất trong dãy Anken là Etilen: CH2 = CH2
>>> Xem thêm: Lý Thuyết Ankadien Hóa 11: Định Nghĩa, Tính Chất Và Điều Chế Ankadien
Dãy đồng đẳng của anken
Etilen (CH2 = CH2) và các chất kế tiếp có công thức phân tử là C3H6, C4H8, C5H10,… Chúng có tính chất tương tự etilen và lập thành dãy đồng đẳng có công thức phân tử chung là CnH2n (n > 2) được gọi là anken hoặc olefin.
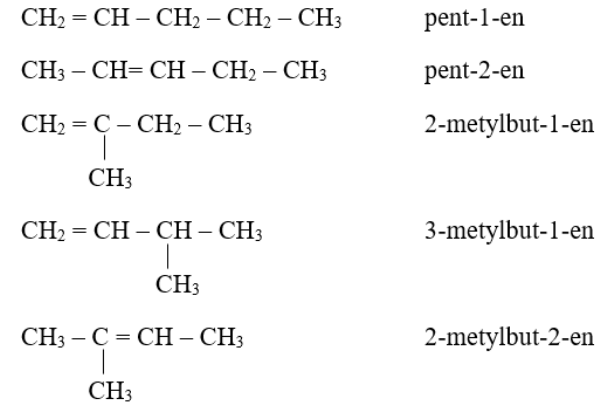
Đồng phân của anken
- Đồng phân cấu tạo:
- Đồng phân ở vị trí liên kết đôi
CH2 = CH – CH2 – CH3
CH2 – CH = CH – CH3
- Đồng phân mạch cacbon:
Dưới dây là ví dụ về đồng phân mạch cacbon của C5H10:
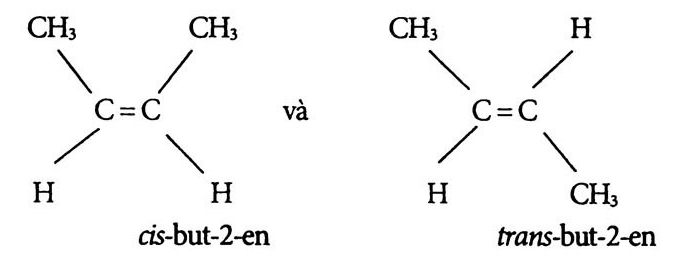
- Đồng phân hình học:
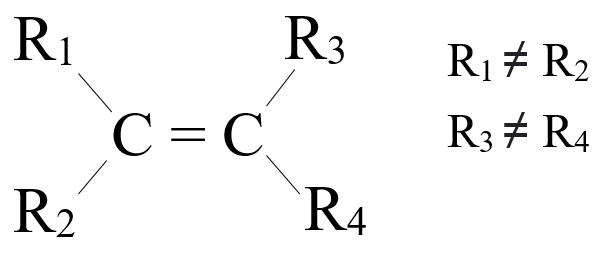
- Đồng phân cis: Khi mạch chính nằm tại vị trí cùng một phía với liên kết C=C.
- Đồng phân trans: Khi mạch chính nằm tại vị trí khác phía với liên kết C=C.
Danh pháp của anken
- Tên thông thường:
Cách gọi tên thông thường của anken: Tên anken = Tên ankan nhưng đổi đuổi an thành đuôi ilen.
Ví dụ: CH2 = CH2 gọi là Etilen
CH2 = CH – CH3 gọi là Propilen
- Tên thay thế:
Cách gọi tên thay thế: Tên anken = Tên ankan và đổi đuôi an thành en.
Quy tắc:
- Chọn mạch C dài nhất và có chứa liên kết đôi làm mạch chính.
- Đánh số C mạch chính từ phía có vị trí gần liên kết đôi nhất.
- Gọi tên theo thứ tự như sau: Số chỉ vị trí nhánh + Tên nhánh + Tên C mạch chính + Số chỉ liên kết đôi + en.
Ví dụ:
CH2 = CH2: Eten
CH3 – CH = CH – CH3: But-2-en
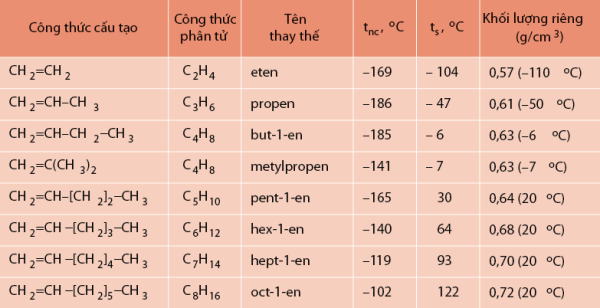
Tính chất vật lý của anken
Anken có một số tính chất vật lý như sau:
- Ở điều kiện thường, từ C2H4 đến C4H8 là chất khí và từ C5H10 trở đi là chất rắn hoặc chất lỏng.
- Nhiệt độ sôi, nhiệt độ nóng chảy và khối lượng riêng của các anken sẽ tăng dần theo chiều tăng của phân tử khối.
- Không tan trong trước và đều nhẹ hơn nước (D < 1 g/cm3).
Tính chất hóa học của anken
Phản ứng cộng
Phản ứng cộng là phản ứng phân tử hợp chất hữu cơ sẽ kết hợp phân tử khác tạo nên phân tử hợp chất mới.
- Cộng hidro (Phản ứng hidro hóa):
C_nH_{2n} + H_2 \xrightarrow{t^o} C_nH_{2n+2}\\
CH_2 = CH_2 + H_2 \xrightarrow{t^o}CH_3 - CH_3\\
CH_3 - CH = CH_2 + H2\xrightarrow{t^o} CH_3 - CH_2 - CH_3
- Cộng halogen (Phản ứng halogen hóa):
C_nH_{2n} + Br_2 \xrightarrow{t^o}C_nH_{2n}Br_2\\
C_2H_4 + Br_2 \xrightarrow{t^o} C_2H_4Br_2\\
C_3H_6 + Br_2 \xrightarrow{t^o} C_3H_6Br_2
Hiện tượng: làm mất màu dung dịch brom → Dùng phản ứng này để nhận biết anken.
- Cộng HX (X là Cl, Oh, Br,…)
Đối với các phản ứng cộng HX vào hidrocacbon không no, các em cần nắm rõ quy tắc cộng HX hay còn được gọi là Quy tắc Maccopnhicop (Markovnikov) sau:
- Nguyên tử H sẽ gắn với nguyên tử cacbon bậc thấp, cụ thể là C ở liên kết đôi có nhiều H hơn.
- Nhóm halide (X) sẽ gắn với nguyên tử cacbon bậc cao, cụ thể là C ở liên kết đôi có ít H hơn.
- Sản phẩm chính của phản ứng chính là sản phẩm được tạo thành theo quy tắc Maccopnhicop.
Ví dụ:
\begin{aligned}
&CH_2 = CH_2 + HBr → CH_3 - CH_2Br\\
&CH_2 = CH_2 + H-OH\xrightarrow{H^+}CH_3 - CH_2OH\\
&CH_3-CH=CH_2+HBr \to CH_3-CHBr-CH_3 \small\text{ (2 - brompropan: sản phẩm chính)}\\
&CH_3-CH=CH_2+HBr \to CH_3-CH_2-CH_2Br \small\text{ (1 - brompropan: sản phẩm phụ)}\\
\end{aligned}
Phản ứng trùng hợp
nCH_2=CH_2\xrightarrow{t^o,\ p, \ xt}\sout{\ [\ }CH_2-CH_2\sout{\ ]\ }_n
Trong đó, chất đầu (CH2 = CH2) là monome, -CH2 – CH2– là mắc xích của polime, n là hệ số trùng hợp.
Phản ứng trùng hợp là sự kết hợp liên tiếp của nhiều phân tử nhỏ tương tự hoặc giống nhau, tạo nên những rất tử rất lớn gọi là polime.
Tên của polime = poli + tên của monome.
Phản ứng oxi hóa
- Oxi hóa hoàn toàn:
C_nH_{2n}+\frac{3n}{2}O_2\xrightarrow{t^o}nCO_2+nH_2O
Trong phản ứng oxi hóa hoàn toàn, số mol của H2O = số mol của CO2.
- Oxi hóa không hoàn toàn:

Phản ứng trên dùng để nhận biết anken vì hợp chất này có thể làm mất màu dung dịch KMnO4.
>>> Xem thêm: Lý Thuyết Về Oxi Và Tính Chất Hóa Học Của Oxi Hóa Lớp 10
Cách điều chế anken
- Trong phòng thí nghiệm:
Etilen sẽ được điều chế từ ancol etylic theo phương trình như sau:
C_2H_5OH\xrightarrow{H_2SO_4,\ 170^oC}CH_2=CH_2+H_2O
- Trong công nghiệp:
Anken còn được điều chế từ ankan theo phương trình:
C_nH_{2n+2} \xrightarrow{t^o,\ p, \ xt}C_nH_{2n}+H_2
Ứng dụng của Anken
- Anken được dùng để chế tạo màng mỏng, bình chứa, ống dẫn nước,… bằng cách trùng hợp etilen, propilen, butilen,… thu được polime
- Anken được ứng dụng để sản xuất rượu, dẫn xuất halogen và một số chất khác
- Monome được chuyển hóa từ Etilen để tổng hợp hàng loạt polime đáp ứng nhu cầu phong phú của đời sống, kĩ thuật
Giải một số bài tập sách giáo khoa
Bài 1 trang 132 SGK
Viết các phương trình hóa học minh họa:
a) Để tách metan từ hỗn hợp với một lượng nhỏ etilen, người ta dẫn hỗn hợp khí đi qua dung dịch brom dư
b) Sục khí propilen vào dung dịch KMnO4, thấy màu của dung dịch nhạt dần có kết tủa màu nâu đen xuất hiện
Giải:
a) Khi\space dẫn\space hỗn\space hợp\space khí\space (gồm\space CH_4\space và\space C_2H_4)\space qua\space dung\space dịch\space brom\space dư\space thì\space C_2H_4\space sẽ\space\\ tác\space dụng\space với\space dung\space dịch\space nước\space brom,\space CH_4\space không\space tác\space dụng\space sẽ\space đi\space ra\space khỏi\space bình\space được\space dung\space\\ dịch\space nước\space brom\space, PTHH\space như\space sau:
CH_2=CH_2+Br_2\to CH_2Br-CH_2Br
\begin{aligned}
&b)PTHH\space khi\space sục\space khí\space propilen\space C_3H_6\space vào\space dung\space dịch\space KMnO_4\\
&3CH_2=CH-CH_3+2KMnO_4+4H_2O\to 3CH_2(OH)-CH(OH)-CH_3+2MnO_2\downarrow +2KOH
&
\end{aligned}
Bài 6 trang 132 SGK
Dẫn từ từ 3,36 lít hỗn hợp gồm etilen và propilen (đktc) vào dung dịch brom thấy dung dịch bị nhạt màu và không có khí thoát ra. Khối lượng dung dịch sau phản ứng tăng 4,9gam.
a) Viết các phương trình hóa học và giải thích các hiện tượng ở thí nghiệm trên
b) Tính thành phần phần trăm về thể tích của mỗi khí trong hỗn hợp ban đầu
Giải:
a) Các phương trình hóa học sau phản ứng:
\begin{aligned}
& CH_2=CH_2+Br_2 \rarr CH_2Br-CH_2Br\\
&CH_2=CH-CH_3+Br_2\rarr CH_2Br-CHBr-CH_3
\end{aligned}
Giải thích: Dung dịch brom bị nhạt màu do brom phản ứng với hỗn hợp tạo thành hợp chất không màu. Chất lỏng tạo thành làm cho khối lượng bình tăng
b)
Gọi x và y lần lượt là số mol của
C_2H_4 {,}C_3H_6
Ta có 3,36l hỗn hợp gồm etilen và propilen: x+y = (3,36/22,4) = 0,15 (1)
Khối lượng dung dịch sau phản ứng tăng 4,9gram chính là khối lượng của etilen và propen cho vào nên: 28x+42y=4,9 (2)
Từ (1) và (2) ta có hệ phương trình:
\begin{cases}
&n_{hh}=x+y=0,15\\
&m_{hh}=28x+42y=4,9
\end{cases}
\\
=>x=0,1mol,y=0,05mol\\
=>V\%C_2H_4= 66,7\%\\
=>V\%C_3H_6=33,3\%
Tham khảo ngay các khoá học online của Marathon Education
Trên đây là chia sẻ về các kiến thức cơ bản về anken. Hy vọng với các thông tin hữu ích trên sẽ giúp các em có thêm tự tin trong việc học môn Hóa. Chúc các em học online thật tốt và đạt được nhiều thành quả cao!
Các Bài Viết Liên Quan