Anđehit Là Gì? Tính Chất Lý Hóa Và Công Thức Của Anđehit
Trong chương trình Hóa học 11, các em sẽ được làm quen với các hợp chất hữu cơ có tên là Anđehit. Các hợp chất này đóng vai trò quan trọng trong đời sống và là nguyên liệu cho một số ngành sản xuất công nghiệp. Vậy Andehit là gì? Công thức của Anđehit là gì? Hợp chất này có những tính chất vật lý và tính chất hóa học nào? Trong bài viết này, Team Marathon Education sẽ cùng các em tìm hiểu đầy đủ và chi tiết về lý thuyết này.
Anđehit là gì?
Anđehit là các hợp chất hữu cơ trong phân tử có nhóm –CH=O liên kết với nguyên tử cacbon hoặc nguyên tử hidro. Nói cách khác, Andehit chính là sản phẩm thu được sau khi thay thế nguyên tử H trong hiđrocacbon hoặc H2 bằng nhóm –CHO.
Nhóm –CH=O có tên gọi là nhóm chức của Andehit.
Các ví dụ về Andehit:
HCH=O: Anđehit Fomic hoặc Metanal
CH3CH=O: Anđehit Axetic hoặc Etanal
C6H5CH=O: Anđehit Benzoic hoặc Benzanđehit
O=CH-CH=O: Anđehit Oxalic
>>> Xem thêm: Anđehit Acrylic là gì? Công thức hóa học và tính chất
Công thức của Anđehit
Công thức cấu tạo của Anđehit
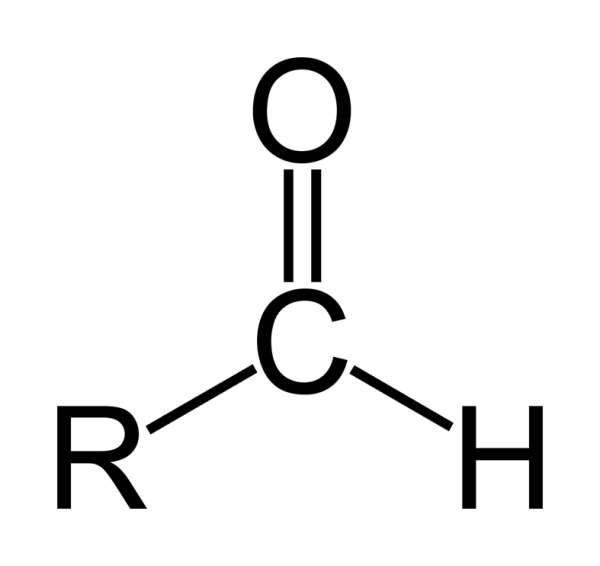
Công thức tổng quát của Anđehit
- CxHyOz (trong đó x, y, z là các số nguyên dương và y là số chẵn thỏa mãn điều kiện 2 ≤ y ≤ 2x + 2 – 2z và z ≤ x): Công thức này thường dùng để viết phản ứng cháy.
- CxHy(CHO)z hay R(CHO)z: Công thức này thường được dùng để viết phản ứng xảy ra ở nhóm CHO.
- CnH2n+2-2k-z(CHO)z (k = số liên kết p + số vòng): Công thức này thường được dùng khi viết phản ứng cộng H2 hay cộng Br2…
Phân loại Anđehit
Anđehit được chia thành 5 loại khác nhau tùy theo đặc điểm cấu tạo của gốc hidrocacbon và số nhóm –CHO trong phân tử.
- Dựa vào cấu tạo của gốc hidrocacbon: Andehit no, Andehit không no và Andehit thơm
- Dựa vào số nhóm –CHO: Andehit đơn chức và Andehit đa chức
Ví dụ:
CH3−CH=O: Anđehit no
CH2=CH−CH=O: Anđehit không no
C6H5-CH=O: Anđehit thơm
Công thức của Anđehit theo phân loại trên:
- Andehit no, đơn chức, mạch hở: CnH2n+1CHO (n≥0) hoặc CmH2mO (m≥1)
- Andehit no, đa chức, mạch hở: CnH2n(CHO)2 (n≥0) hoặc CmH2m-2O2 (m≥2)
- Andehit không no, chứa nối đôi C=C, đơn chức mạch hở: CmH2m-2O (m≥3)
Danh pháp Anđehit
Tên thông thường
Tên thường = Anđehit + Tên axit tương ứng
Tên thay thế
- Chọn mạch C dài nhất chứa nhóm -CHO làm mạch chính
- Đánh số từ nhóm -CHO
Tên thay thế = Tên hidrocacbon tương ứng + al
Bảng danh pháp Andehit phổ biến
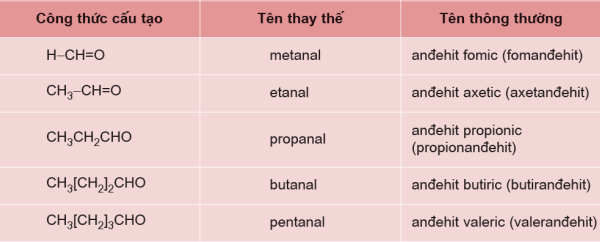
Ngoài ra, các em cũng cần chú ý một hợp chất đặc biệt trong cách gọi tên. Dung dịch HCHO 37% – 40% thì được gọi là fomalin hay fomon.
Đặc điểm cấu tạo và tính chất vật lý của Anđehit
Đặc điểm cấu tạo của Anđehit
- Anđehit có chứa nhóm chức –CH=O.
- Trong nhóm chức này, liên kết C=O bao gồm một liên kết σ bền và một liên kết π kém bền. Do đó, hợp chất này có tính chất khá giống với anken (tính oxy hóa và tính khử).
Tính chất vật lý của Anđehit
- Nhiệt độ sôi: Nhiệt độ sôi của Anđehit thấp hơn Ancol có cùng khối lượng do không có liên kết hidro trong phân tử (chỉ có nhóm –CH=O không có nhóm –OH) và cao hơn hidrocacbon có cùng số nguyên tử C.
- Trạng thái: Trong điều kiện thường, các chất đầu dãy đồng đẳng như HCHO, CH3CHO là chất khí, tan trong nước. Các chất còn lại là chất lỏng hoặc chất rắn. Phân tử khối của hợp chất càng lớn thì độ tan trong nước càng giảm.
- Dung dịch HCHO trong nước được gọi là fomon, dung dịch có nồng độ 37% – 40% gọi là fomalin.
Tính chất hóa học của Anđehit
1. Phản ứng cộng hiđro
Trong điều kiện nhiệt độ và chất xúc tác Ni:
R(CHO)_x+xH_2\xrightarrow[Ni]{t^\circ}R(CH_2OH)_x
Lưu ý:
- Khi Anđehit tác dụng với H2, nếu gốc R có liên kết π thì H2 sẽ cộng vào các liên kết π đó.
- Anđehit khi phản ứng với H2 có vai trò là chất oxi hóa.
2. Phản ứng oxi hóa
- Phản ứng oxi hóa hoàn toàn:
C_xH_yO_z+(x+\frac{y}{4}-\frac{z}{2})O_2 \to xCO_2\ +\frac{y}{2}H_2O
Khi bị đốt cháy mà nCO2 = nH2O thì Anđehit đó thuộc loại no, đơn chức hoặc mạch hở.
C_nH_{2n+1}CHO \to (n + 1)CO_2 + (n + 1)H_2O
- Phản ứng oxi hóa không hoàn toàn:
R(CHO)_x\ +\frac{x}{2}O_2\xrightarrow[Mn^{2+}]{t^\circ} R(COOH)_x
3. Phản ứng với AgNO3/NH3 (Phản ứng tráng bạc)
\scriptsize{R(CHO)_x + 2xAgNO_3 + 3xNH_3 + xH_2O \to R(COONH_4)_x + xNH_4NO_3 + 2xAg}
Phản ứng này chứng minh được Anđehit có tính khử và có thể áp dụng để nhận biết hợp chất này.
Lưu ý:
- Cứ 1 nhóm CHO sẽ sinh ra 2 Ag.
- Riêng HCHO có phản ứng:
\scriptsize{HCHO + 4AgNO_3 + 2H_2O + 6NH_3 \to (NH_4)_2CO_3 + 4NH_4NO_3 + 4Ag\downarrow}
4. Phản ứng với Cu(OH)2
Trong môi trường kiềm và nhiệt độ:
\scriptsize{R(CHO)_x + 2xCu(OH)_2 + xNaOH → R(COONa)_x + xCu_2O + 3xH_2O}
Phản ứng này làm xuất hiện kết tủa đỏ gạch và thường được sử dụng để nhận biết Anđehit.
5. Phản ứng với Br2
R(CHO)_x + xBr_2 + xH_2O → R(COOH)_x + 2xHBr
- Anđehit làm mất màu nước Brom.
- 1 nhóm CHO phản ứng với 1 Br2.
- Riêng HCHO sẽ có phản ứng:
HCHO + 2Br_2 + H_2O \to CO_2 + 4HBr
Cách điều chế Anđehit
Điều chế Anđehit từ Ancol
- Oxi hóa Ancol bậc I sẽ thu được Anđehit tương ứng.
- Trong công nghiệp, Metanal được điều chế bằng cách oxi hóa Metanol nhờ oxi không khí trong điều kiện nhiệt độ từ 600−700 độ C cùng chất xúc tác là Cu hoặc Ag.
2CH_3−OH + O_2 \xrightarrow[Ag]{600^{\circ}} H−CH=O + 2H_2O
Điều chế Anđehit từ hidrocacbon
- Oxi hóa metan có xúc tác và nhiệt độ sẽ thu được Anđehit Fomic.
- Theo phương pháp hiện đại, oxi hoá không hoàn toàn etilen sẽ thu được Anđehit Axetic.
- Điều chế Axetilen bằng phản ứng cộng nước thu được Anđehit Axetic.
Một số ứng dụng của Anđehit

Anđehit được ứng dụng rộng rãi trong các hoạt động sản xuất công nghiệp như:
- Fomanđehit dùng để sản xuất nhựa Poliphenolfomanđehit.
- Fomanđehit có nồng độ 37 – 40% (Fomon hay Fomalin) được dùng để ngâm xác động vật, diệt trùng, tẩy uế,…
- Axetanđehit được dùng trong sản xuất Axit Axetic.
Tham khảo ngay các khoá học online của Marathon Education
Thông qua bài viết này, Team Marathon Education đã tổng hợp kiến thức về Andehit là gì, công thức của Anđehit cũng như tính chất lý hóa, cách điều chế và ứng dụng… Hy vọng sau khi đọc xong bài viết, các em có thể vận dụng những kiến thức này để làm tốt các bài tập hóa học liên quan đến hợp chất này. Chúc các em học online thật tốt tại Marathon Education và luôn dành được điểm cao!
Các Bài Viết Liên Quan